DIPOL Fälle NCH
Fall 1 - Neuroonkologie
Fall 2 - Vaskuläre Neurochirurgie
Fall 3 - Neuroonkologie
Fall 4 - Schmerzen der Hand
Fall 5 - Bandscheibenvorfall LWS
Fall 6 - Neuroonkologie (Low-Grade Gliom)
Information, Datenschutz und Impressum
Schließen
Das Bildmaterial für diese WebApp wurde unter anderen aus folgenden Quellen mit freien Lizenzen
acquiriert:
- http://www.cancerimagingarchive.net/ - MRT
vom Tumor, F1
- Radiopaedia
- Radiopaedia - Prof. Frank Gillard (Abszess F1, Glioblastom F3 - MRT, postoperative Bilder, HWS
F4)
- Radiopaedia - Prof. Peter Mitchell (SAB CT, F2)
- Radiopaedia - Dr. Hani Salam (Tumor CT, F3)
- Kim
YB, Hong CK, Chung J, Joo JY, Huh SK - Yonsei Med. J. (2014) auf Pubmed Central - F2,
Aneurysma, DSA und Fotos (geändert, angepasst)
- Radiopaedia - Bandscheibenvorfall LWS (F5), Fall rID-86776, lizenziert unter CC BY-NC-SA
3.0
- Radiopaedia - Thibodeau R, Oligodendroglioma (F6). Case study, Radiopaedia.org, https://doi.org/10.53347/rID-166550,
lizenziert unter CC
BY-NC-SA 3.0
Schließen
Impressum Angaben gemäß § 5 TMG:
PD Dr. med. Amir Zolal
Flemmingstr. 2
09116 Chemnitz
Kontakt:
Telefon: 0371 333 0
EMail:
amir.zolal@skc.de
Haftung für Inhalte
Als Diensteanbieter
sind wir gemäß § 7 Abs.1 TMG für eigene Inhalte auf diesen Seiten nach den
allgemeinen Gesetzen verantwortlich. Nach §§ 8 bis 10 TMG sind wir als Diensteanbieter
jedoch nicht verpflichtet, übermittelte oder gespeicherte fremde Informationen zu
überwachen
oder nach Umständen zu forschen, die auf eine rechtswidrige Tätigkeit hinweisen.
Verpflichtungen zur Entfernung oder Sperrung der Nutzung von Informationen nach den allgemeinen
Gesetzen bleiben hiervon unberührt. Eine diesbezügliche Haftung ist jedoch erst ab dem
Zeitpunkt der Kenntnis einer konkreten Rechtsverletzung möglich. Bei Bekanntwerden von
entsprechenden Rechtsverletzungen werden wir diese Inhalte umgehend entfernen.
Haftung
für Links
Unser Angebot enthält Links zu externen Webseiten Dritter, auf deren
Inhalte wir keinen Einfluss haben. Deshalb können wir für diese fremden Inhalte auch keine
Gewähr übernehmen. Für die Inhalte der verlinkten Seiten ist stets der jeweilige
Anbieter
oder Betreiber der Seiten verantwortlich. Die verlinkten Seiten wurden zum Zeitpunkt der Verlinkung
auf
mögliche Rechtsverstöße überprüft. Rechtswidrige Inhalte waren zum
Zeitpunkt der Verlinkung nicht erkennbar.
Eine permanente inhaltliche Kontrolle der verlinkten
Seiten ist jedoch ohne konkrete Anhaltspunkte einer Rechtsverletzung nicht zumutbar. Bei
Bekanntwerden von Rechtsverletzungen werden wir derartige Links umgehend entfernen.
Urheberrecht
Die durch die Seitenbetreiber erstellten Inhalte und Werke auf diesen Seiten
unterliegen dem deutschen Urheberrecht. Die Vervielfältigung, Bearbeitung, Verbreitung und jede
Art der Verwertung außerhalb der Grenzen des Urheberrechtes bedürfen der schriftlichen
Zustimmung des jeweiligen Autors bzw. Erstellers. Downloads und Kopien dieser Seite sind nur
für
den privaten, nicht kommerziellen Gebrauch gestattet.
Soweit die Inhalte auf dieser Seite nicht
vom Betreiber erstellt wurden, werden die Urheberrechte Dritter beachtet. Insbesondere werden
Inhalte
Dritter als solche gekennzeichnet. Sollten Sie trotzdem auf eine Urheberrechtsverletzung aufmerksam
werden, bitten wir um einen entsprechenden Hinweis. Bei Bekanntwerden von Rechtsverletzungen
werden wir derartige Inhalte umgehend entfernen.
Lösungen für Dozenten (Alle Lernpunkte) anzeigen
Schließen
Datenschutzerklärung Datenschutz
Die Betreiber dieser Seiten nehmen
den Schutz Ihrer persönlichen Daten sehr ernst. Wir behandeln Ihre personenbezogenen Daten
vertraulich und entsprechend der gesetzlichen Datenschutzvorschriften sowie dieser
Datenschutzerklärung.
Die Nutzung unserer Webseite ist in der Regel ohne Angabe
personenbezogener Daten möglich. Soweit auf unseren Seiten personenbezogene Daten
(beispielsweise Name, Anschrift oder E-Mail-Adressen) erhoben werden, erfolgt dies, soweit
möglich, stets auf freiwilliger Basis. Diese Daten werden ohne Ihre ausdrückliche
Zustimmung
nicht an Dritte weitergegeben.
Wir weisen darauf hin, dass die Datenübertragung im Internet
(z.B. bei der Kommunikation per E-Mail) Sicherheitslücken aufweisen kann. Ein lückenloser
Schutz der Daten vor dem Zugriff durch Dritte ist nicht möglich.
Schließen
Herr Gross ist ein Verkehrspolizist. In den letzten 2 Monaten hat er vermehrt Kopschmerzen
bemerkt, welche er der hohen Arbeitsbelastung und dem Stress zugeschrieben hat. Eines Morgens am Dienstag
fing der linke Arm plötzlich an zu Zucken. Die Zuckung hat von alleine aufgehört, allerdings war der Arm
nachher "komisch". Herr Gross hat daraus vorerst nichts gemacht und ging bis Freitag ganz normal auf Arbeit.
Am Samstag nach dem Frühstück hat der Arm wieder angefangen zu zucken. Diesmal hat die Zuckung nicht
aufgehört, sondern sich auf den ganzen Körper verbreitet. Herr Gross wurde bewusstlos und die Frau hat den
Rettungsdienst alarmiert.
Der Notarzt Dr. Schmidt sah einen 56-jährigen Patienten, somnolent aber orientiert. Pupillen
isokor, mittelweit mit erhaltener Lichtreaktion. Ausserdem wurde eine leichte Hemiparese links festgestellt
(Absinktendenz im Armhalteversuch). Keine Pyramidrnbahnzeichen. Kein Sturz oder sonstiges Kopftrauma in den
letzten 3 Monaten erinnerlich. Der Notarzt hat sich entschieden, den Patienten im Klinikum Freital zu
weiterer Untersuchung vorzustellen. Es wird gleich eine Flexüle gelegt. Die Ehefrau des Patienten fragt Dr.
Schmidt nach möglichen Ursachen des Zustandes.
Lernpunkte
Close
Lernpunkte:
1. Abklärung des erstmaligen epileptischen Krampfanfalls im Erwachsenenalter -
AWMF Leitlinie
2. Wie würde man die Anfälle vor dem jetztigen Anfall beschreiben?
3. Wie würde man den aktuellen Anfall beschreiben?
4. Kann eine Hemiparese durch einen Krampfanfall entstehen?
5. Warum ist ein Transport ins Krankenhaus indiziert?
Im Krankenhaus Freital wird der Patient durch Dr. Klein untersucht, zuerst wird ein natives
CT des Kopfes durchgeführt. Das Blut, was der Notarzt schon während der Fahrt abgenommen hat, wird ins Labor
geschickt.
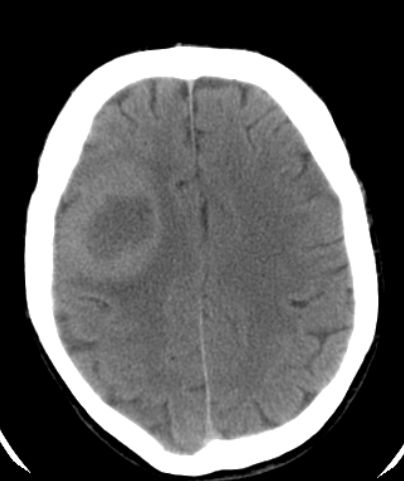
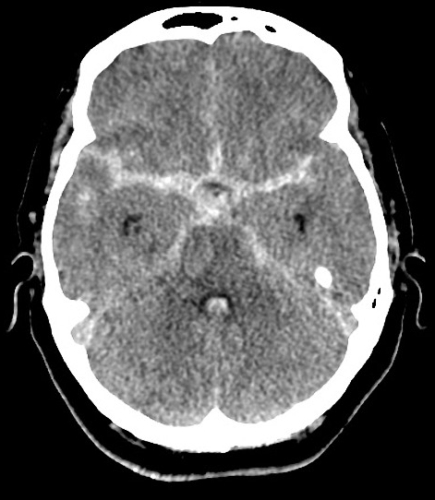
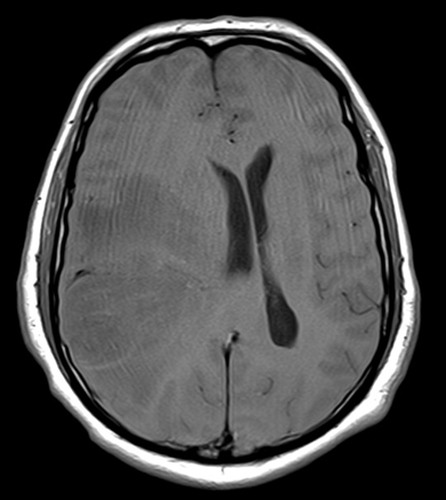
Der Kurzbefund vom CT lautet:
Eine intraaxiale, rundliche, ca 3,5 cm große Raumforderung im rechten Frontallappen, zentral
hypodens, mit mäßigem Perifokalödem. Kein Anhalt für eine Einblutung. Keine Verkalkungen. Dringend MRT und
neurochirurgische Vorstellung empfohlen.
Nach der Untersuchung wartet Herr Gross in der Notaufnahme auf Dr. Klein. Plötzlich ruft die
Schwester den jungen Assistenzarzt. "Herr Dr. Klein, der Patient krampft!"
Der Patient liegt am Bett und der linke Arm zuckt unwillkürlich. Nun muss der Arzt entscheiden, welche
Behandlungsmaßnahmen notwendig sind.
CT Bild
Lernpunkte
Close
Lernpunkte:
1. Akute Behandlung des epileptischen Krampfanfalls?
2. Interpretation des CT Befundes? (s. Bild) inkl. Differentialdiagnosen?
3. Wie sieht eine Blutung im Hirn aus? (Google
Image Suche)
4. Kann man anhand von diesem CT schon operieren?
Es wurden 2 mg Tavor i.v. verabreicht. Nach der Gabe des Medikamentes sistiert die Zuckung, allerdings ist
der Patient jetzt somnolent. Er reagiert nun auf Ansprache mit Augenöffnen und unverständlichen Worten. Dr.
Klein ist unsicher, ob der Patient nun doch nicht zur Atemwegsicherung intubiert werden sollte. Er ruft
seinen Oberarzt an, der jedoch beim erweckbaren Patienten mit GCS über 8 keine Intubation empfiehlt.
Mittlerweile sind Ergebnisse aus dem Labor gekommen:
|
Erythrozyten
|
5.1 x 10^6 / mm³
|
|
Leukozyten
|
8,9 x 10^3 / mm³
|
|
Thrombozyten
|
212 x 10^3 / mm3
|
|
CRP
|
22 mg / l
|
Der Rest des Befundes ist unauffällig.
Dr. Klein vereinbart jetzt mit der diensthabenden Neurochirurgin der Uniklinik Dresden, Frau Dr. Müller, die
Verlegung des Patienten.
Lernpunkte
Close
Lernpunkte:
1. Wodurch kann eine Vigilanzminderung nach einem Krampfanfall verursacht werden?
2. Kann man anhand des Laboregebnisses ein Hirnabszess schon ausschliessen? (PubMed)
3. Bei welchem GCS wäre die Indikation zur Intubation für den Transport gegeben?
4. Was begründet die Indikation zum notfallmäßigen Transport in die Neurochirurgie?
Frau Dr. Müller bespricht die Befunde mit Dr. Klein und empfiehlt ihm nach wiederholtem epileptischen Anfall
die Gabe von 1000 mg Levetiracetam (Keppra) als Kurzinfusion. Nach dem Gespräch ruft sie die chirurgische
Notaufnahme des Uniklinikums an: „Es kommt ein Patient aus dem Krankenhaus Freital, nicht intubiert,
somnolent, unter dem Verdacht auf Hirnabszess, differenzialdiagnostisch Hirntumor.“ Zudem organisiert Sie
für den Patienten ein Bett auf der Intensivstation und bespricht mit den Kollegen der Neuroradiologie eine
zusätzliche Untersuchung, die noch am Aufnahmetag notwendig wird.
Nach dem Eintreffen des Patienten in die Notaufnahme ist der Patient schon voll wach und orientiert. Die
linksseitige Hemiparese ist jetzt ausgeprägt. Es erfolgt die Aufnahme auf die Zentralchirurgische
Intensivstation zur Überwachung. Außerdem wartet der Patient auf die angemeldete Untersuchung. Der
behandelnde Arzt der Intensivstation, Dr. Falken, ruft die Dienstärztin Dr. Müller an und möchte wissen,
welche Untersuchung genau angemeldet werden soll und warum die Untersuchung notwendig ist.
Lernpunkte
Close
Lernpunkte:
1. Wie lautet die moderne Definition der Epilepsie (ILAE 2014)? Kann die Diagnose bei diesem Patienten
schon bestätigt werden?
2. Was ist der aktuelle Fachbegriff für die veraltete Bezeichnung "symptomatische Epilepsie" (Tipp:
strukturelle Ätiologie)?
3. Warum ist die Hemiparese jetzt mehr ausgeprägt als vorher?
4. Ist bei jedem neu diagnostizierten Hirntumor die Überwachung auf der Intensivstation notwendig?
5. Welche Untersuchung soll noch am gleichen Abend stattfinden?
Bitte entscheiden Sie, mit welcher der Differentialdiagnosen der Fall fortgesetzt wird
Frau Dr. Müller bestätigt dem Kollegen die Notwendigkeit der Untersuchung, da es sich bis jetzt nur um einen
Verdacht auf Hirnabszess handelt. Sollte sich der Verdacht im MRT nicht bestätigen, ist keine notfallmäßige
Operation am Abend oder in der Nacht indiziert. Trotzdem werden zwei Blutkulturen abgenommen. Zusätzlich zu
der diagnostischen Untersuchung soll eine Hochauflösungs-Sequenz in T1-Wichtung mit Kontrastmittel gemessen
werden.
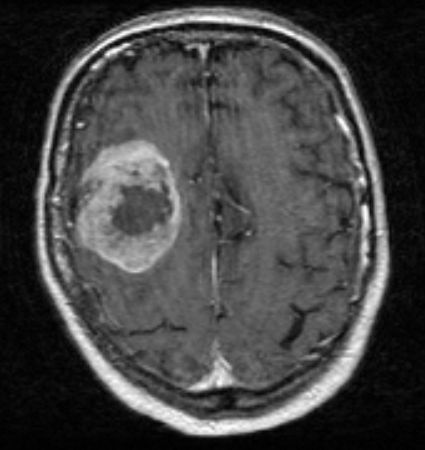
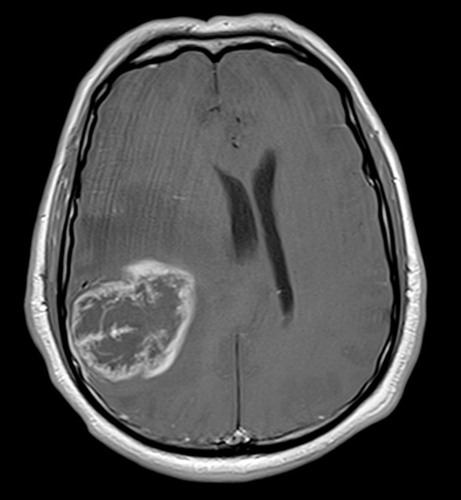
Die Untersuchung wird 16:30 Uhr durchgeführt. Der vorläufige Kurzbefund lautet:
Es findet sich eine Raumforderung im rechen Frontalllappen, noch vor dem Gyrus praecentralis. Der Befund ist
zentralnekrotisch, inhomogen mit randständiger Schrankenstörung. Die diffusionsgewichteten Sequenzen zeigen
keine Diffusionsstörung im zentralnekrotischen Teil der Raumforderung, so dass ein Abszess eher
unwahrscheinlich ist. Differenzialdiagnostisch kommt ein höhergradiger hirneigener Tumor oder eine Metastase
in Frage. Ein Lymphom erscheint weniger wahrscheinlich.
Frau Dr. Müller bespricht den Befund mit ihrem Oberarzt, Prof. Apfelbaum. Da der MRT - Befund nicht für
einen Abszess spricht, kann der Patient auf die Normalstation übernommen werden.
Hier wird zusätzlich eine Dexamethasontherapie mit 2 x 8 mg (morgens und mittags) unter Magenschutz
mit Pantozol 40
mg 1-0-0, sowie Thromboseprophylaxe mit niedermolekularem Heparin s.c. eingeleitet.
Frau Dr. Müller klärt den Patienten über die Verdachtsdiagnose eines Hirntumors auf und bietet ihm eine
operative Behandlung an. Der Patient entscheidet sich für die Operation und bleibt auf der
neurochirurgischen Normalstation. Er möchte aber wissen, ob die Möglichkeit besteht, dass der Befund
gutartig ist. Darüber möchte Frau Dr. Müller aufgrund der fehlenden histologischen Sicherung keine Auskunft
geben.
Es wird die Operation vorbereitet und die entsprechende Einverständniserklärung vom Patienten erhoben. Am
Operationstag wird um 6 Uhr morgens dem Patienten 5-ALA (5-Aminolävulinsäure, Gliolan) zum Einnehmen
gegeben.
MRT Bild
Lernpunkte
Close
Lernpunkte:
1. Weswegen wird Dexamethason gegeben?
2. Was für ursächlichen Typen des Hirnödems werden unterschieden?
3. Kann ein zytotoxisches Ödem gut mit Kortikoiden beeinflusst werden?
4. Klassifikation der ZNS-Tumore (2021). (online)
5. Wozu dient die Hochauflösungssequenz, die aufgenommen worden ist?
Die Operation wird nach entsprechender Vorbereitung mit Hilfe von Neuronavigation, elektrophysiologischem
Monitoring und Fluoreszenz unter blauem Licht (400 nm) durchgeführt. Intraoperativ zeigt der Tumor eine
deutliche Fluoreszenz, was für einen höhergradigen hirnegenen Tumor spricht. Als malignes Gliom wird der
Tumor auch im Schnellschnitt beschrieben.
Nach einer Woche kommt der definitive histologische Befund. Es handelt sich um ein Glioblastom, CNS
WHO Grad 4. Eine Methylierung des MGMT-Promotors ist nicht vorhanden, IDH1 – Mutation ist ebenfalls negativ.
Der Fall wird im interdisziplinären Tumorboard besprochen, es wird eine RCTx nach Stupp – Schema empfohlen.
Der Fall wird als palliativ eingestuft.
Lernpunkte
Close
Lernpunkte:
1. Wozu dient die intraoperative Elektrophysiologie? Wie wird die durchgeführt?
2. Welche Rolle spielt die MGMT-Methylierung für die Prognose? IDH-Mutation?
3. Wie wird die Radiochemotherapie nach Stupp-Schema durchgeführt?
4. Welche weitere zugelassene Therapieoption (z.B. Tumor Treating Fields / TTFields) kann ergänzend als
Erhaltungstherapie eingesetzt werden?
Frau Dr. Müller bestätigt dem Kollegen die Notwendigkeit der Untersuchung, da es sich bis jetzt nur um einen
Verdacht auf Hirnabszess handelt. Sollte sich der Verdacht im MRT nicht bestätigen, ist keine notfallmäßige
Operation am Abend oder in der Nacht indiziert. Trotzdem werden zwei Blutkulturen abgenommen. Zusätzlich zu
der diagnostischen Untersuchung soll eine Hochauflösungs-Sequenz in T1-Wichtung mit Kontrastmittel gemessen
werden.
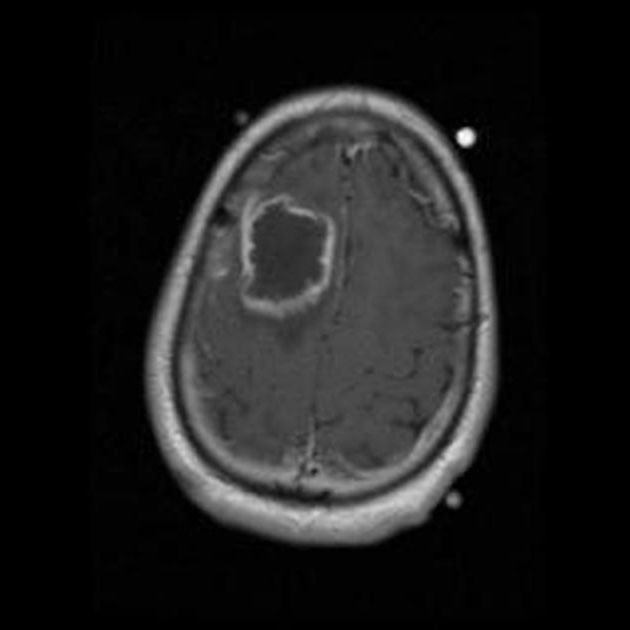
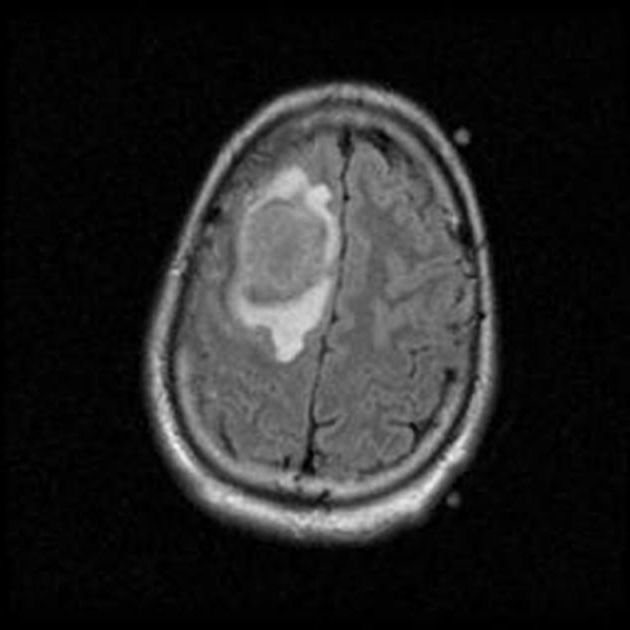
Die Untersuchung wird 16:30 Uhr durchgeführt. Der vorläufige Kurzbefund lautet:
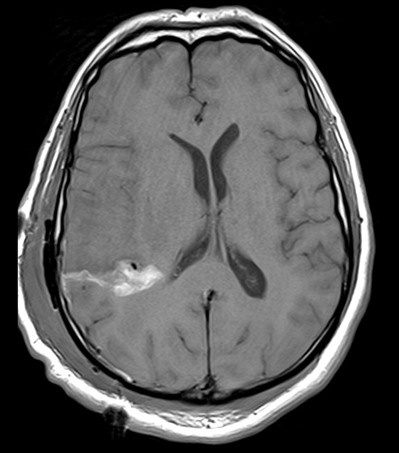
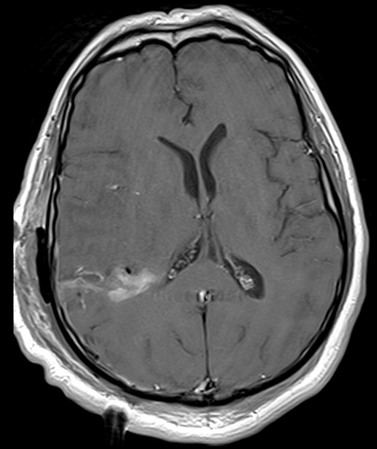
Es findet sich eine Raumforderung im rechen Frontalllappen, noch vor dem Gyrus praecentralis. Der Befund
zeigt sich in der DWI als diffusionsgestört, daher besteht ein dringender Verdacht auf Hirnabszess. Befund
telefonisch an Dr. Müller übergeben.
Frau Dr. Müller bespricht den Befund mit ihrem Oberarzt, Prof. Apfelbaum. Es wird eine nofallmäßige
Operation indiziert. Prof. Apfelbaum bereitet die Neuronavigation mit der Trajektorie zur navigierten
Punktion des Abszesses vor. Eine Antibiose wird vorerst nicht gegeben.
MRT Bild - T1+C
MRT Bild - FLAIR
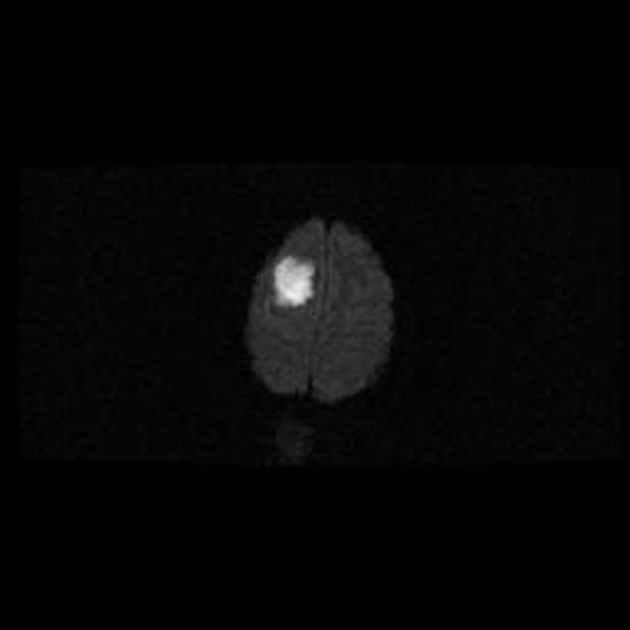
MRT Bild - DWI
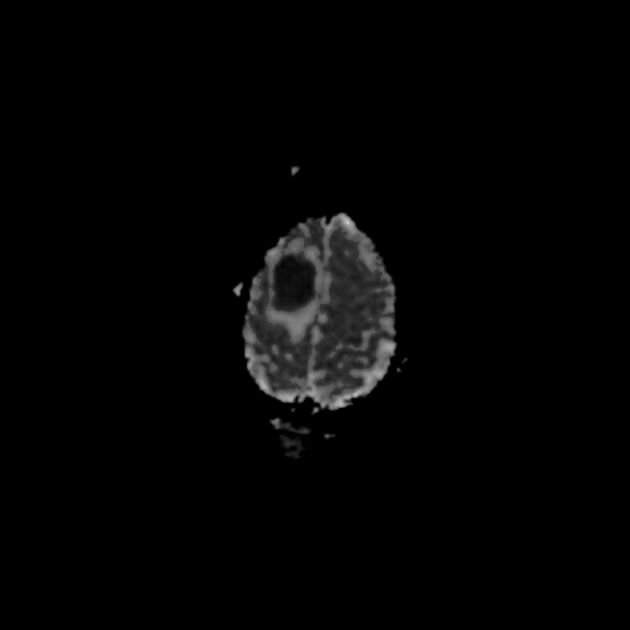
MRT Bild - ADC
Lernpunkte
Close
Lernpunkte:
1. Weswegen wird keine Antibiose vor der Operation verabreicht?
2. Was ist der häufigste Erreger beim Hirnabszess?
3. Welche weiteren Untersuchungen sind im Rahmen der Fokussuche indiziert?
4. Wie lange soll ein Hirnabszess mit Antibiotika behandelt werden?
5. Risikofaktoren Hirnabszess?
Die Operation wird nach entsprechender Vorbereitung mit Hilfe der Neuronavigation durchgeführt. Über ein
Bohrloch wird eine Drainage in den Abszess eingeführt. Es entleert sich Eiter, das Material wird in die
Mikrobiologie eingeschickt. Die Drainage wird mit ca 5 ml Gentamicin (1 mg / ml) angespült und in der
Abszesshöhle belassen.
Die Sofortmikroskopie zeigt keine Keime. Der Patient wird zunächst empirisch leitliniengemäß
mit i.v. Ceftriaxon in Kombination mit Metronidazol und Flucloxacillin behandelt.
Lernpunkte
Close
Lernpunkte:
1. Wie lange dauert die antibiotische Behandlung bei einem Hirnabszess?
2. In welchen Fällen kann eventuell eine rein nichtoperative Behandlung (antibiotisch) überlegt werden?
3. In welchen Fällen wäre eine Resektion des Abszesses (anstelle von Drainage) indiziert?
Frau Müller ist 46 Jahre, verheiratet und hat 2 Söhne. Sie arbeitet als Büroangestellte in einer
Versicherungsfirma, ihr Mann Rainer als Ingenieur, ist aber sehr selten zu Hause. Wie an jedem Morgen sitzt
Frau Müller mit ihren beiden Söhnen am Frühstückstisch und schmiert die Brote für die Schule.
Plötzlich verspürt sie einen heftigen Kopfschmerz am Hinterkopf, wie er noch nie aufgetreten war. Sie leidet
seit langer Zeit schon an Migräne und denkt, es sei wieder eine solche Attacke. Wie jedes Mal nimmt Frau
Müller eine Tablette Paracetamol, wovon die Symptomatik etwas besser wird. Sie legt sich erst einmal hin um
sich zu entspannen, doch die Kopfschmerzen wollen nicht aufhören. Obwohl sie nichts gegessen hat verspürt
sie Übelkeit und muss sich übergeben. Sie bittet ihren Sohn, den Notarzt zu informieren. Nach einiger Zeit
ist der Notarzt, Dr. Hartmann, eingetroffen und befragt Frau Müller. Sie berichtet über das plötzliche
Kopfschmerzereignis und die Übelkeit mit Erbrechen. Bei der körperlichen Untersuchung fällt dem Notarzt eine
ausgeprägte Nackensteifigkeit auf. Weitere neurologische Ausfälle findet er nicht. Dr. Hartmann informiert
den diensthabenden Neurologen einer Klinik und stellt die Patientin dort vor.
Lernpunkte
Close
Lernpunkte:
1. Was sind die typischen Leitsymptome einer Subarachnoidalblutung (SAB)?
2. Welche klinischen Skalen werden zur Einschätzung des Schweregrads einer SAB genutzt (z.B. Hunt &
Hess, WFNS)?
3. Was sind die ersten diagnostischen Schritte bei Verdacht auf SAB?
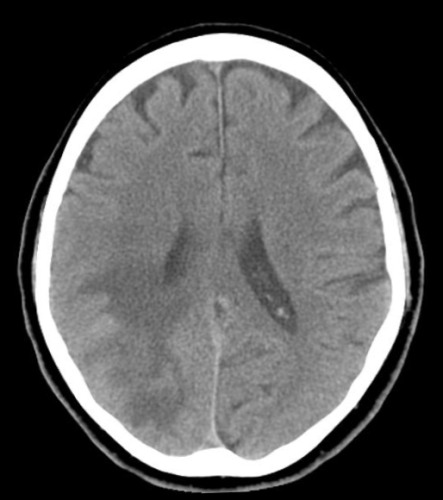
Der diensthabende Neurologe, Dr. Steffen, veranlasst eine Computertomographie des Kopfes. Der Kurzbefund
lautet:
Es findet sich eine Blutung in den basalen Zisternen, sowie in den Sylvischen Fissuren bds.
Da der Verdacht besteht, dass es sich hierbei um eine Aneurysmablutung handelt, wird Frau Dr. Hoffmann, die
diensthabende Neurochirurgin, hinzugerufen. Für sie ist die Sache klar und übernimmt die Patientin auf die
neurochirurgische Wachstation, legt der Patientin einen zentralvenösen Zugang und eine arterielle
Druckmessung zur kontinuierlichen Blutdrucküberwachung. Sie informiert die Schwester und bittet sie den
Blutdruck engmaschig zu kontrollieren, welcher systolisch nicht höher als 160 mmHg sein sollte, um eine
Reblutung zu vermeiden, ohne die Perfusion zu gefährden. Des Weiteren setzt die
Ärztin einen spezifischen Kalziumantagonisten für Hirnarterien (Nimodipin) in Tablettenform (bzw. über
Magensonde) an.
CT Bild
Lernpunkte
Close
Lernpunkte:
1. Wie wird das Ausmaß der Blutung im CT klassifiziert (Fisher-Graduierung)?
2. Welcher Kalziumantagonist wird verabreicht und was ist das genaue Ziel dieser Therapie?
3. Warum wird der Blutdruck in der Akutphase vor Aneurysma-Ausschaltung systolisch auf unter 160 mmHg
eingestellt?
4. Warum wird der Kalziumantagonist Nimodipin laut Leitlinie vorzugsweise oral und nicht intravenös
gegeben?
5. Was ist die nächste diagnostische Maßnahme bei weiterhin hochgradigem klinischen Verdacht auf eine SAB, wenn das CT unauffällig (negativ) ist?
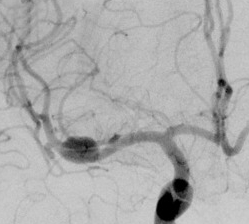
Dr. Albers, ein Neuroradiologe, wird darüber informiert, dass eine Angiographie der intrakraniellen Gefäße
durchgeführt werden soll. In dieser bestätigt sich nun der Verdacht einer Aneurysmablutung. Es zeigt sich
ein Bifurkationsaneurysma ausgehend von der Arteria cerebri media links, welches aus neuroradiologischer
Sicht laut Dr. Albers interventionell durch Coiling nicht versorgt werden kann, da es direkt in der Gabel
der Aufteilungstelle liegt, einen relativ breiten Hals aufweist und einen peripheren Mediaast mit
einbezieht.
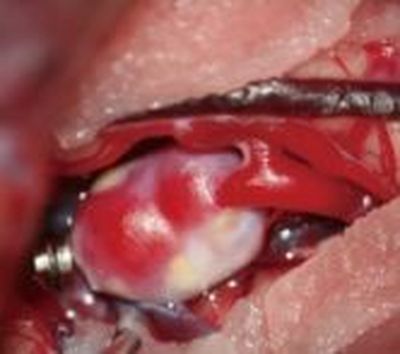
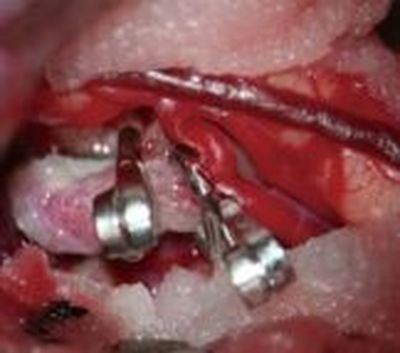
Nachdem der Befund der Angiographie vorhanden ist, bespricht Frau Dr. Hoffmann die operative Vorgehensweise
und die möglichen Komplikationen mit Frau Müller. Vereinbarungsgemäß wird die Patientin am nächsten Tag
operativ über eine osteoplastische Trepanation durch Aneurysma-Clipping versorgt.
DSA
Aneurysma vor dem Clipping
Aneurysma mit Clips
Lernpunkte
Close
Lernpunkte:
1. Welche Faktoren sprechen für ein mikrochirurgisches Clipping und welche für ein endovaskuläres
Coiling?
2. Was ist die Rolle der Digitalen Subtraktionsangiographie (DSA) in der Diagnostik und
Therapieplanung?
Frau Müller hat die Operation gut überstanden und wird 3 Tage später auf die neurochirurgische Wachstation
verlegt. Wegen der möglichen Risiken eines Vasospasmus werden täglich von Frau Dr. Hoffmann transkranielle
Doppleruntersuchungen durchgeführt, die im weiteren Verlauf keine Flussbeschleunigungen zeigen.
Leitliniengerecht achtet die Ärztin streng auf eine Normovolämie der Patientin und führt die prophylaktische
Gabe von Nimodipin weiter fort.
Neurologische Auffälligkeiten der Patientin ergeben sich nicht. Sie ist noch sehr schwach, kann aber reden
und alle Extremitäten bewegen.
Eines Morgens fällt der Schwester auf, dass Frau Müller auf Ansprache nicht antwortet und eine
Schwäche der rechten Körperhälfte aufweist. Auch an diesem Tag hat Frau Dr. Hoffmann wieder Dienst. Sie
veranlasst sofort eine Computertomographie, in der sich kein Infarkt oder eine Nachblutung zeigt.
Lernpunkte
Close
Lernpunkte:
1. In welchem Zeitfenster nach der Blutung treten zerebrale Vasospasmen am häufigsten auf?
2. Wozu dient die transkranielle Dopplersonographie (TCD) auf der Intensivstation?
3. Welche Differentialdiagnosen müssen bei einer plötzlichen neurologischen Verschlechterung nach SAB
ausgeschlossen werden (z.B. Hydrozephalus, Reblutung, Infarkt)?
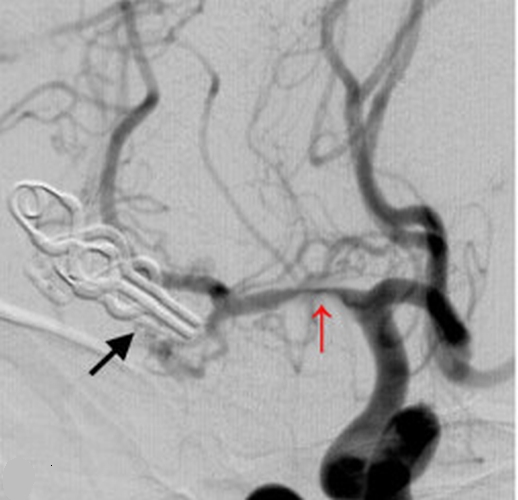
Anschließend wird nach Rücksprache mit dem diensthabenden Neuroradiologen erneut eine Angiographie
durchgeführt, in der sich ein ausgeprägter Vasospasmus darstellt. Das Aneurysma ist nicht mehr nachzuweisen.
Dr. Liebner, ein weiterer Neuroradiologe, entschließt sich zu einer Angioplastie und der lokalen Gabe von
Nimotop.
Frau Müller wird nach der Intervention wieder auf die Intensivstation zur Überwachung zurückverlegt.
Aufgrund des symptomatischen Vasospasmus wird nun eine induzierte Hypertensionstherapie (bei Normovolämie)
begonnen. In den weiteren Tagen kommt es unter logopädischer Betreuung bei Frau Müller zu einer Verbesserung
der Sprache. Auch die rechtsseitige Schwäche ist rückläufig. Vasospasmen sind in der transkraniellen
Dopplersonografie nicht mehr nachzuweisen. Nach 3 wöchigem Aufenthalt in der Klinik kann Frau Müller endlich
in eine Rehaklinik verlegt werden.
Nach 6 Monaten kommt die Patientin zur Kontrolle in die neurochirurgische Ambulanz. Die Ambulanzärztin Frau
Dr. Heller ist erstaunt, wie gut sich Frau Müller in der Rehaklinik erholt hat. Außer einer geringen
kognitiven Leistungsschwäche fallen der Ambulanzärztin keine Besonderheiten auf. Frau Müller erzählt ihr,
dass sie sich sehr gut fühlt und bald wieder anfangen wird zu arbeiten.
DSA
Lernpunkte
Close
Lernpunkte:
1. Wie wird ein symptomatischer Vasospasmus (DCI) nach aktuellen Leitlinien therapiert (Induzierte
Hypertension)?
2. Wann ist eine endovaskuläre Intervention (Spasmolyse/Angioplastie) indiziert?
3. Wie ist die allgemeine Prognose und Rehabilitation bei Patienten nach SAB und symptomatischem
Vasospasmus?
Herr Sänger ist 52 Jahre alt und von Beruf Bauarbeiter. Er ist ledig, hat aber seit einiger
Zeit wieder eine Freundin. Mit seinen Kollegen vom Bau trifft er sich 1-2mal die Woche im Gasthaus „Zum
Krug“ um Skat zu spielen. Eigentlich wollte Herr Sänger schon längst aufhören zu rauchen, was seine neue
Freundin freuen würde, die vor 4 Jahren aufgehört hat. Doch in der netten Runde wird viel geraucht und
getrunken. Herr Sänger raucht schon seit 35 Jahren. An einem schönen Sommertag steht Herr Sänger morgens auf
und kocht sich einen Kaffee. Es fällt ihm schwer mit der linken Hand die Tasse Kaffe an den Mund zu führen.
Am Bau angekommen, sagt ihm ein Kollege, dass er immer das linke Bein hinterher zieht. Er kommt abends nach
Hause und erzählt seiner Freundin Brigitte, ob ihr das auch aufgefallen sei. Weil Brigitte in Schichten in
ihrem Job arbeitet, sehen sie sich sehr selten. Nachdem er ihr zeigt, welches Problem er mit dem linken Arm
und Bein hat, informiert die Freundin den Notarzt. Herr Sänger wird noch am Abend in ein nahe liegendes
Krankenhaus durch den Notarzt eingeliefert. Der diensthabende Kollege der Rettungsstelle Dr. Huber übernimmt
den Patienten, führt eine körperliche Untersuchung durch, in der ihm eine Hemiparese links auffällt.
Lernpunkte
Close
Lernpunkte:
1. Differenzialdiagnose der Hemiparese
2. Was sind die nächsten diagnostischen Schritte?
Er veranlasst eine Computertomographie des Kopfes. Dr. Huber der Rettungsstellenarzt möchte
einen Infarkt oder eine Blutung ausschießen.
CT Bild
Lernpunkte
Close
Lernpunkte:
1. Was sieht man im CCT?
2. Wie unterscheidet sich eine Blutung von einem Tumor im CT?
3. Google Bilder Suche: CT brain
intracranial hemorrhage
4. Google Bilder Suche: CT brain tumor
5. Google Bilder Suche: CT brain stroke
Im CT zeigt sich eine Raumforderung frontal rechtsseitig mit einem perifokalen Ödem, welches
bis in die Zentralregion hineinreicht. Als Dr. Huber den Befund erhält, informiert er telefonisch den
diensthabenden Neurochirurgen Dr. Seibel, der den Patienten zur operativen Versorgung in die Neurochirurgie
stationär übernimmt. Bei der Anamneseerhebung erzählt Herr Sänger, seit etwa 35 Jahren zu rauchen. Ansonsten
seien keine Vorerkrankungen bekannt. Bei der körperlichen Untersuchung fällt dem Arzt eine leichte
Facialisparese links und eine armbetonte Hemiparese links (obere Extremität KG 2-3/5, untere KG 4/5) auf.
Die Muskeleigenreflexe sind links betont auslösbar. Des Weiteren fällt ein Klonus des linken Fußes auf.
Lernpunkte
Close
Lernpunkte:
1. Was ist der nächste diagnostische Schritt?
2. Differenzialdiagnose zu diesem Zeitpunkt?
Wegen des ausgedehnten Ödems beginnt Dr. Seidel mit einer Dexamethasontherapie. Um eine
genauere Gewebeauflösung zu erhalten, wird eine MRT-Untersuchung mit Kontrastmittel durchgeführt. In dieser
zeigt sich ein ausgedehnter Tumor rechts im Bereich der rechten Zentralregion.
Herr Sänger wird darüber informiert, dass es sich bei ihm um einen Tumor im Kopf handle und eine Operation
durchgeführt werden muss. Der Patient wird genauestens über die möglichen Risiken der Operation aufgeklärt
und ist mit dem Eingriff einverstanden.
MRT Bild - ohne KM
MRT Bild - mit KM
Lernpunkte
Close
Lernpunkte:
1. Was sind die Risiken der Operation?
2. Wie würde man die Lage des Tumors beschreiben?
3. Welche wichtigen Hirnregionen befinden sich in der Nähe des Tumors?
4. Gibt es andere Therapiemöglichkeiten außer Operation?
5. Wie läuft die präoperative Vorbereitung?
5. Bei welchen Erkrankungen wird Dexamethason zur Behandlung des Hirnödems angesetzt?
5. Welche anderen Medikamente können zur Behandlung des Hirnödems angesetzt werden und wann sind diese
indiziert?
Am nächsten Tag wird die Operation über eine osteoplastische Trepanation und die Extirpation
des Tumors durchgeführt. Intraoperativ zeigt sich ein gefäßreicher Tumor, der vom gesunden Hirngewebe sehr
schlecht abzugrenzen ist. Intraoperativ wird die Fluoreszenz und direkte Stimulation mit intraoperativem
elektrophysiologischem Monitoring angesetzt. Nach der Operation wird Herr Sänger auf die neurochirurgische
Wachstation verlegt.
Lernpunkte
Close
Lernpunkte:
1. Warum wird Fluoreszenz angesetzt und wie funktioniert sie?
2. Wozu dient die Elektrophysiologie?
3. Welche anderen Geräte werden bei der Operation verwendet?
Eine MRT-Untersuchung des Kopfes am Folgetag bestätigt regelrechte Verhältnisse im OP-Gebiet.
Es zeigt sich kein Kontrastmittel aufnehmender Tumor mehr.
Da keine Nachblutungen nachzuweisen sind, kann Herr Sänger auf die Normalstation verlegt werden.
Dem Stationarzt fällt in der neurologischen Untersuchung die weiterhin bestehende Hemiparese auf und spricht
mit dem Patienten darüber, dass der Tumor auch Teile der Pyramindenbahn „zerstört“ hat, die für die Bewegung
zuständig ist und dies wohl so bleiben wird. Nach 7 Tagen bespricht Dr. Seidel den histologischen Befund mit
dem Patienten. Dabei sagt er ihm, dass es sich um einen hirneigenen Tumor handelt, der sehr schnell wächst,
sodass eine weitere Therapie durchgeführt werden muss. In der neurochirurgischen-strahlentherapeutischen
Konferenz wird der Fall besprochen und es wird beschlossen bei dieser Art von Tumor, einem Glioblastom,
IDH-Wildtyp, CNS WHO Grad 4 mit MGMT-Methylierung, eine kombinierte Radiochemotherapie (Stupp-Schema)
durchzuführen. Nach dem
08. postoperativen Tag wird Herr Sänger nach Hause entlassen. Währen der nächsten Woche findet ein Gespräch
in der Klinik für Strahlentherapie statt, bei dem die weitere Therapie (ambulante Strahlentherapie mit
gleichzeitiger Chemotherapie) geplant wird.
Postoperatives MRT Bild - ohne KM
Postoperatives MRT Bild - mit KM
Lernpunkte
Close
Lernpunkte:
1. Welche Rolle spielt das Ausmaß der Resektion für die Prognose?
2. Warum soll die postoperative MRT-Untersuchung innerhalb von 72h nach der Operation erfolgen?
3. Welche molekulargenetischen Merkmale sind nach der WHO-Klassifikation von 2021 für die Diagnose eines
Glioblastoms obligat (z.B. IDH-Wildtyp)?
4. Spielen die genetischen Merkmale (wie die MGMT-Promotor-Methylierung) eine Rolle bei der
Therapieentscheidung?
Frau Trautenberg arbeitete als Lehrerin, ist aber schon seit zwei Jahren in der Rente. Sie
genießt vor allem die Zeit, die sie in ihrem Kleingarten verbringen kann. Sie leidet seit Jahren an
Nackenschmerzen. Seit zwei Monaten verspürt sie gelegentlich Kribbeln und Taubheit im Daumen der rechten
Hand, ab und zu Kribbeln auch im Zeigefinger und im Mittelfinger. Sie kann sich erinnern, dass Sie ungefähr
in der Zeit, wo die Beschwerden angefangen haben, vom Fahrrad gestürzt ist. Die Kribbelparästhesien werden
mit der Zeit mehr und mehr unangenehm und sind mit schmerzhaften Gefühlen verbunden. Sie entscheidet sich,
zum Hausarzt zu gehen.
Lernpunkte
Close
Lernpunkte:
1. Differenzialdiagnose der Kribbelparästhesien.
2. Differenzialdiagnose zwischen Radikulopathie und Neuropathie anhand klinischer Untersuchung.
Frau Trautenberg stellt sich mit den Beschwerden bei ihrem Hausarzt vor. Der Hausarzt, Dr.
Jäger, fragt sie nach der Intensität der Schmerzen. Sie gibt an, in Ruhe Schmerzen in der Intensität von 2
der visuellen Analogskala (VAS) zu spüren, bei Belastung gibt sie die 4 an. Das Kribbeln und die Schmerzen
wecken sie manchmal in der Nacht, sie hat das Gefühl, dass sie manchmal falsch liegt, dann kommen die
Schmerzen. Der Hausarzt führt die klinische Untersuchung durch.
Bei der stellt er die folgende Befundkonstellation fest:
A. Hypästhesie der Volarseite der Finger I-IV rechts, sowie der volaren Handoberfläche mit gestörter
Zwei-Punkt-Diskriminierung, Schmerzen aber auch im Unterarm und Oberarm. Zudem positives Tinel - Zeichen am
Handgelenk rechts, positives Phalen-Zeichen, seitengleiche Muskeleigenreflexe, keine Paresen.
B. Schmerzen der Finger I-III rechts, nicht scharf abgegrenzt, die Patientin beschreibt das Einschießen in
die Nackenmuskulatur, keine Muskelschwäche, Abschwächung des Bizepssehnenreflexes und des
Radius-Periost-Reflexes rechts im Vergleich zur Gegenseite, der Trizepssehnenreflex erscheint eher stärker
als links, obwohl dies nicht eindeutig ist. Es besteht eine eindeutige Steigerung der MER der rechten
unteren Extremität im Vergleich zu links. Phalen-Zeichen und Tinel-Zeichen bleiben
negativ.
Lernpunkte
Close
Lernpunkte:
1. Verdachtsdiagnosen beim Fall A / B?
2. Die nächsten diagnostischen Schritte?
Dr. Jäger informiert die Patientin über die Verdachtsdiagnose eines Karpaltunnelsyndroms. Es folgt eine
Überweisung zu einem Spezialisten zur Komplettierung der Diagnostik. Es wird eine Handgelenkschiene
verschrieben, die Frau Trautenberg in der Nacht tragen soll. Der Hausarzt informiert allerdings die
Patientin, dass die konservative Therapie mittels Schienung meist nur vorübergehende Verbesserung der
Symptomatik erzielen kann und die Verzögerung der definitiven Therapie nicht unbedingt vorteilhaft ist
(Nervenschäden sind nur zum Teil reversibel).
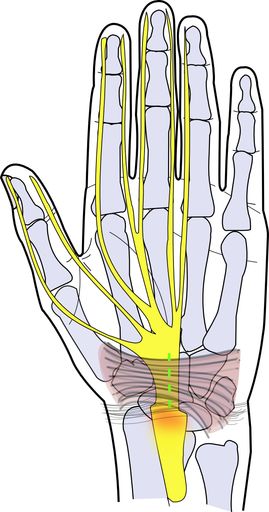
Sensibles Versorgungsgebiet N.
medianus
Lernpunkte
Close
Lernpunkte:
1. Wie lange soll die konservative Therapie versucht werden (allgemein und in diesem Fall)? (AWMF Leitlinie)?
2. Was sind die Voraussetzungen für die Beendigung des konservativen Therapieversuchs? Sind die hier
erfüllt?
Die elektrophysiologische Untersuchung beim niedergelassenen Neurologen zeigt den folgenden Befund:
Die motorische Neurographie zeigt eine erhöhte distal-motorische Latenz am rechten N. medianus im Vergleich
zu den Referenzwerten. Links sind die Latenzen grenzwertig. In der sensiblen Neurographie zeigt sich eine
Verlangsamung der Nervenleitgeschwindigkeit auf 35 m/s, verglichen mit der NLG von 58 m/s am rechten N.
ulnaris. Auch hier ist links der Befund grenzwertig mit NLG von 48 m/s. Somit bestätigt sich das klinisch
vermutete Karpaltunnelsyndrom rechts.
Lernpunkte
Close
Lernpunkte:
1. Welche weiteren Untersuchungen sind präoperativ erforderlich?
2. Welche konservative / operative Therapiemethoden gibt es?
Herr Dr. Jäger überweist die Patientin in die Klinik für Neurochirurgie zur Beurteilung der
Operationsindikation. Herr Dr. Zimmermann empfängt sie in der Ambulanz für Chirurgie der peripheren Nerven.
Er informiert die Patientin über die Therapiemöglichkeiten, die Patientin entscheidet sich aufgrund der doch
leicht erhöhten Komplikationsrate bei der endoskopischen Operation für die Goldstandard-Methode im Sinne
einer offenen Karpaltunneloperation. Sie wird noch während des Erstgesprächs für die Operation aufgeklärt,
der Arzt nimmt ihr das Blut ab und plant die ambulante Operation in der Tagesklinik.
Lernpunkte
Close
Lernpunkte:
1. Welche anatomische Struktur wird bei der Operation des Karpaltunnelsyndroms gespalten?
2. Was sind die Vor- und Nachteile der offenen vs. endoskopischen Karpaltunnelspaltung?
3. Warum wird dieser Eingriff in der Regel ambulant durchgeführt?
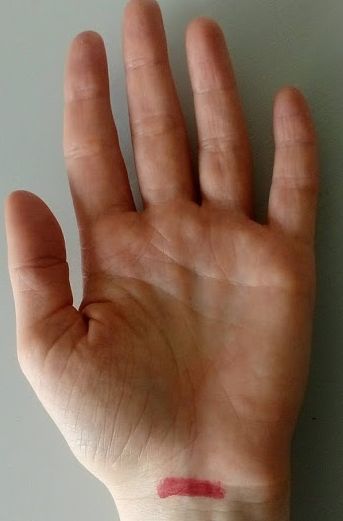
Hautschnitt bei der offenen Operation
Hautschnitt bei der endoskopischen
Operation
Die Operation erfolgt in einer Woche. Herr Dr. Zimmermann informiert die Patientin, dass die Operation ca
10-15 Minuten dauern wird. Der Arm wird auf dem Armtisch ausgelagert, die Operation wird in einer
Armplexusanästhesie komplikationslos durchgeführt. Das Ziel der Operation ist die komplette Spaltung des
Ligamentum carpi transversum, die durch einen kurzen Schnitt durchgeführt werden kann. Nach der Spaltung des
Ligamentum carpi transversum (Retinaculum flexorum) von einem ca 3 cm langen Schnitt in der Hohlhand zeigt
sich ein komplett dekomprimierter Nerv. Die Wunde wird mit 5-0 Fäden verschlossen.
Schematische OP-Darstellung
Lernpunkte
Close
Lernpunkte:
1. Welche Behandlung soll nach der Operation verordnet werden? (Ergotherapie?)
2. Welche Symptome sind nach der Operation rasch regredient und welche können länger verbleiben?
(Reizsymptome - Kribbeln und Schmerzen / Ausfallsymptome - Hypästhesie und Parese)
3. Was bedeutet das Wort “Pseudoneurom”?
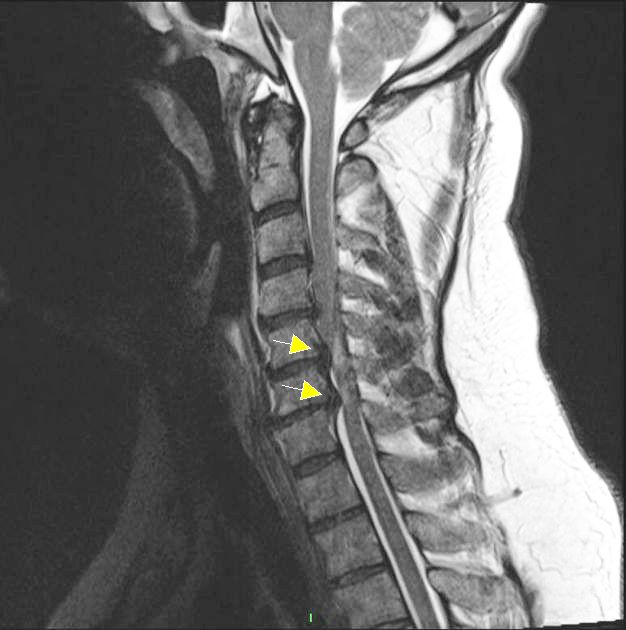
Beim V.a. Radikulopathie C6 rechts veranlasst Dr. Jäger ein MRT der HWS in einer radiologische Praxis. Die
Befundung kommt etwa 14 Tage später und lautet:
… Konstitutiv enger Spinalkanal …
… Osteochondrose HWK5/6 mit breitbasigem Bandscheibenvorfall paramedian rechts, Foramenstenose bds.
rechtsbetont. Spinalkanalstenose mit T2-Myelopathiesignal in dieser Etage, keine Veränderung des T1-Signals
…
… Osteochondrose HWK6/7 mit breitbasigem Bandscheibenvorfall, auch hier rechtsbetont, Spinalkanalstenose mit
T2-Myelopathiesignal, allerdings geringer als in der Etage HWK5/6 keine Veränderung des T1-Signals …
Herr Dr. Jäger überweist die Patientin in die Klinik für Neurochirurgie mit Bitte um Beurteilung der
Operationsindikation.
MRT Bild - T2 Sagittal
Lernpunkte
Close
Lernpunkte:
1. Was bedeutet “T2-Myelopathiesignal”?
2. Wie würde sich ein motorischer Ausfall der C6-Wurzel äußern?
Frau Dr. Schreiber in der neurochirurgischen Ambulanz liest den Bericht des Hausarztes und führt eine
neurologische Untersuchung durch, die im Wesentlichen den Befund des Hausarztes bestätigt. Sie berät die
Patientin bezüglich des Befundes und informiert sie, dass es sich um keinen Notfall handelt, dass man
allerdings aufgrund der relativ rasch progredienten Symptomatik (Beginn vor ca 2 Monaten) bei nachgewiesener
T2-Signalanhebung die Operation empfiehlt. Die Patientin möchte nun wissen, wie die Operation durchgeführt
wird.
Lernpunkte
Close
Lernpunkte:
1. Welchen Zugang wählen wir üblicherweise bei HWS-Operationen?
2. Gibt es andere möglichkeiten der Behandlung?
Frau Dr. Schreiber erklärt der Patientin, dass die Operation vom ventralen Zugang durchgeführt wird. Durch
diese Operation kann der Bandscheibenvorfall entfernt werden und gleichzeitig die in die Foramina
eingehenden Osteophyten durchgeführt werden. Eine dorsale Dekompression wäre wegen des Druckes von ventral
nicht das optimale Vorgehen. Sie klärt die Patientin über die möglichen Risiken der Operation auf. Die Frage
der Patientin nach einer Bandscheibenprothese wird diskutiert, bei einer nachgewiesenen Myelopathie in 2
Etagen wird dies allerdings nicht empfohlen. Die Patientin bekommt einen Aufnahmetermin in die Klinik in ca
2 Wochen.
Lernpunkte
Close
Lernpunkte:
1. Wie genau wird die Operation mit dem ventralen Zugang durchgeführt?
Am Aufnahmetag wird die Patientin für die Operation aufgeklärt. Es wird das Aufnahmelabor abgenommen und
eine umfangreiche Aufnamheuntersuchung durchgeführt. Bei der Operation werden die Bandscheiben, sowie die
Osteophyten an den Wirbelkörpern mittels Fräse und Stanzen entfernt. Die Stenose des Neuroforamens, die die
Beschwerden der Patientin verursacht hat, war vor allem durch die Osteophyten bedingt. Als Platzhalter
werden PEEK-Cages (Polyetheretherketon) implantiert, die die Höhe des Segmentes halten sollen und
gleichzeitig eine Fusion der Wirbelkörper ermöglichen sollen. Eine Verplattung wird beim festen Sitz der
Cages nicht notwendig. Es wird eine Drainage in die Wunde eingelegt und die Wunde schichtweise verschlossen.
Postoperativ berichtet die Patientin von einer deutlichen Schmerzlinderung vor allem im Arm und in der Hand,
die Nackenschmerzen sind zwar besser geworden, sind aber noch nicht ganz weg. Die behandelnde
Assistenzärztin klärt die Patientin auf, dass die Nackenschmerzen nicht unbedingt durch die
Spinalkanalstenose verursacht werden, und dass eine weitere Rehabilitation mit Stärkung der Nackenmuskulatur
notwendig wird. Die Patientin ist zufrieden. Die Drainage wird am zweiten postoperativen Tag entfernt, die
Patientin kann am 5. postoperativen Tag entlassen werden.
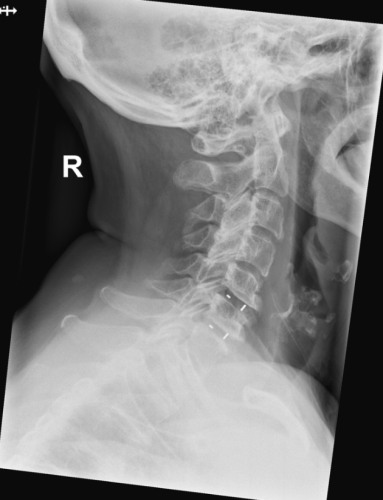
Postoperative Röntgenaufnahme
Lernpunkte
Close
Lernpunkte:
1. Sind nach der Operation passive Manipulationen an der HWS erlaubt?
Herr Richter, ein 45-jähriger selbstständiger Handwerker, krümmt sich vor Schmerzen, als er die Praxis
seines Hausarztes betritt.
"Herr Doktor, so kann ich nicht arbeiten. Jeder Schritt zieht wie ein elektrischer Schlag über die
Außenseite meines Beins bis runter in die große Zehe! Ich kann doch nicht wochenlang krankfeiern, meine
Kunden warten!"
Der Arzt untersucht ihn beruhigend. Da der Lasègue-Test zwar bei 40 Grad schmerzhaft positiv ist, aber
glücklicherweise noch keine Lähmungserscheinungen bestehen, erklärt der Arzt:
"Ich verstehe Ihre Sorge um den Betrieb, Herr Richter. Die gute Nachricht ist: Etwa 80 Prozent der
Bandscheibenvorfälle heilen ohne Operation aus. Wir versuchen es zunächst mit starken Schmerzmitteln und
Physiotherapie."
Lernpunkte
Close
Lernpunkte:
1. Für welche Nervenwurzel ist die Schmerzausstrahlung (Außenseite Unterschenkel bis Großzehe)
typisch?
2. Wie lange kann oder soll man laut Leitlinie die konservative Behandlung bei einem unkomplizierten
Bandscheibenvorfall durchführen (ohne absolute OP-Indikation)?
Trotz Schonung und Physiotherapie kommt es vier Wochen später an einem Montagmorgen zur Katastrophe. Herr
Richter will sich seine Arbeitsschuhe binden, als ein furchtbar stechender Schmerz durch seinen Rücken
schießt.
Kurz darauf breitet sich ein Taubheitsgefühl auf dem Fußrücken aus. Als er versuchen will zu gehen, knickt
er fast um – sein rechter Fuß hängt schlaff herab ("Steppergang").
Panik steigt in ihm auf. Seine Frau fackelt nicht lange, packt ihn ins Auto und fährt ihn direkt in die
Notaufnahme.
Dort zeigt sich bei der Untersuchung durch den jungen diensthabenden Neurochirurgen eine deutliche
Fußheberparese (nur noch Kraftgrad 2/5).
Lernpunkte
Close
Lernpunkte:
1. Welche klinischen Zeichen stellen eine absolute OP-Indikation ("Red Flag") beim Bandscheibenvorfall
dar?
2. Welcher Muskel ist bei einer L5-Parese primär für die Fußhebung verantwortlich (M. tibialis
anterior)?
Der Arzt fackelt nicht lange und schiebt Herrn Richter als Notfall sofort ins MRT. Herr Richter ist
schweißgebadet vor Schmerz und sichtlich verängstigt.
Wenig später sitzt der Neurochirurg mit ihm vor dem Monitor. "Sehen Sie diesen großen schwarzen Brocken
hier?", erklärt der Arzt und zeigt auf die Bilder.
"Das ist ein riesiger abgerissener Teil Ihrer Bandscheibe – ein sogenannter Sequester. Er drückt den
L5-Nerv, der für die Fußhebung zuständig ist, komplett ab."
MRT LWS sagittal
MRT LWS axial
Lernpunkte
Close
Lernpunkte:
1. Wie lautet der MRT-Befund genau?
2. Was ist der Unterschied zwischen einer Protrusion, einem Prolaps und einem Sequester?
Herr Richter wehrt ab: "Eine Rücken-OP? Auf keinen Fall, da landet man doch im Rollstuhl!"
Der Neurochirurg setzt sich zu ihm und wird sehr ernst: "Herr Richter, Ihre Fußhebung ist fast komplett
ausgefallen. Das ist eine 'Red Flag', ein absoluter Notfall. Wenn wir diesen Nerv nicht innerhalb der
nächsten Stunden entlasten, bleibt Ihr Fuß womöglich für immer lahm. Dann können Sie das Gerüstbauen als
Handwerker tatsächlich vergessen."
Der Gedanke an eine dauerhafte Behinderung überzeugt Herrn Richter schließlich. Er unterschreibt die
Aufklärung und wird direkt in den OP gefahren.
Lernpunkte
Close
Lernpunkte:
1. Warum ist eine hochgradige Parese (< KG 3) ein akuter Notfall?
2. Wie erfolgt der typische chirurgische Zugang zur mikrochirurgischen Sequestrektomie?
Die mikrochirurgische Sequestrektomie verläuft komplikationslos. Als Herr Richter im Aufwachraum langsam die
Augen aufschlägt, stutzt er. Das furchtbare, elektrisierende Ziehen im Bein ist weg!
Zaghaft versucht er, die rechte Fußspitze in Richtung Nase zu ziehen – und es klappt fast so gut wie vorher.
Ihm treten Tränen der Erleichterung in die Augen.
Schon am dritten Tag nach der OP besucht ihn der Operateur zur Abschlussvisite. "Gute Arbeit, wir haben das
Schlimmste verhindert", lächelt er. "Jetzt geht es ab in die Physiotherapie und zur Rückenschule. Wenn Sie
die Übungen durchziehen, können Sie in ein paar Wochen wieder voll auf der Baustelle anpacken."
Lernpunkte
Close
Lernpunkte:
1. Wie ist die Prognose der motorischen Erholung nach Notfall-Dekompression?
2. Welche Nachsorgemaßnahmen (Physiotherapie, Rückenschule) sind nach einer Bandscheibenoperation
wichtig?
Herr Weber, ein 32-jähriger Gymnasiallehrer, war gestern Abend mit Freunden beim Abendessen und hat dabei
drei Gläser Wein getrunken.
Am nächsten Tag in der Schule will er sich in der Pause im Lehrerzimmer auf die nächste Unterrichtsstunde
vorbereiten, als es passiert:
Zuerst verhält er sich komisch, als ob er nicht mehr sprechen könnte, und bringt nur noch wirres Zeug heraus
(Aphasie).
Eine Kollegin beobachtet entsetzt, wie zunächst sein Gesicht, dann sein rechter Arm und schließlich sein
kompletter Körper zu zucken beginnt und er bewusstlos zu Boden stürzt.
Sie alarmiert sofort den Rettungsdienst.
Als der Notarzt eintrifft, findet er einen somnolenten, aber erweckbaren Patienten vor.
Nach dem Transport in die Klinik und einer postiktalen Phase erholt sich Herr Weber zunehmend. Das
notfallmäßig durchgeführte native CCT in der Notaufnahme zeigt keine akute Blutung.
Zur weiteren Abklärung wird eine MRT-Untersuchung des Kopfes veranlasst.
Lernpunkte
Close
Lernpunkte:
1. Was sind die wichtigsten Differenzialdiagnosen eines erstmaligen epileptischen Anfalls im jungen
Erwachsenenalter?
2. Warum ist bei einem erstmaligen Anfall ein MRT des Kopfes (inkl. Kontrastmittel) zwingend
erforderlich?
Im MRT zeigt sich eine ausgedehnte Raumforderung links frontal ohne Kontrastmittelaufnahme, typisch für ein
niedriggradiges Gliom. Der Befund reicht bis an das Sprachzentrum heran.
Herr Weber liegt völlig verunsichert auf der neurochirurgischen Station, seine Frau sitzt weinend an
seiner Seite. Chefarzt Prof. Apfelbaum kommt zur Visite ans Bett.
Auf die ängstliche Frage der Ehefrau, ob der Tumor denn "gut- oder bösartig" sei, antwortet der Professor
behutsam:
"Bilder allein können uns das leider nicht mit absoluter Sicherheit sagen, wir brauchen das Gewebe unter dem
Mikroskop. Aber ich kann Ihnen Mut machen: Selbst wenn es eine bösartige Variante ist, haben wir heute
exzellente Chancen auf ein langes Überleben, sofern wir den Tumor weitreichend entfernen können und die
Genetik günstig ist."
Wenig später betritt die klinische Logopädin das Zimmer. Sie stellt sich freundlich vor und erklärt
dem Ehepaar einfühlsam den genauen Ablauf der bevorstehenden Wach-OP und der Sprachtestung. Das nimmt den
beiden einen großen Teil ihrer Angst.
MRT Kopf sagittal T1 mit KM
MRT Kopf axial FLAIR
Lernpunkte
Close
Lernpunkte:
1. Was sind die typischen MRT-Zeichen eines niedriggradigen Glioms im Gegensatz zu einem
Glioblastom?
2. Welche funktionellen Areale befinden sich klassischerweise links frontal?
Im OP ist es dunkel. Herr Weber erwacht langsam aus der Narkose. Er ist zunächst desorientiert und spürt den
fixierten Kopf, doch dann greift eine warme Hand nach seiner – es ist die Logopädin.
"Hallo Herr Weber, wir sind soweit, wir fangen jetzt an", flüstert sie ihm beruhigend zu. Während der
Chirurg, verdeckt von sterilen Tüchern, hochkonzentriert am Gehirn arbeitet und den Kortex elektrisch
stimuliert, zeigt die Logopädin Herrn Weber Bilder auf einem Tablet.
Er benennt sie flüssig: "Hund... Baum... Auto..." Doch plötzlich stockt er. Er sieht das Bild einer Tasse,
aber das Wort will einfach nicht aus seinem Mund kommen.
"Stopp!", ruft die Logopädin sofort. Der Chirurg nimmt die Elektrode zurück – das Sprachzentrum ist
millimetergenau markiert. Um Herrn Weber eine dauerhafte Sprachstörung zu ersparen, muss der Chirurg
schweren Herzens einen kleinen Tumorrest belassen.
Lernpunkte
Close
Lernpunkte:
1. Was ist die genaue Indikation für eine Wach-OP mit Sprach-Mapping?
2. Welche Rolle übernehmen die klinischen Logopäden im Operationssaal?
3. Warum gilt in der Gliomchirurgie das Prinzip der "maximal sicheren Resektion" (Onkologische
Radikalität vs. Lebensqualität)?
Einige Tage später sitzt Herr Weber auf der Bettkante. Er ist überglücklich, dass er völlig normal sprechen
kann.
Prof. Apfelbaum betritt das Zimmer, in der Hand die Ergebnisse der Gewebeuntersuchung. "Es handelt sich um
ein Oligodendrogliom vom Grad 2", erklärt er.
Die Ehefrau atmet hörbar aus: "Gott sei Dank nur Grad 2! Dann ist ja alles gut!"
Der Professor lächelt sanft, muss aber relativieren: "Das ist in der Tat eine der günstigeren Diagnosen,
insbesondere durch die IDH-Mutation und die 1p/19q-Kodeletion in der Genetik. Dennoch wächst auch ein Grad 2
Tumor irgendwann weiter. Da wir wegen Ihres Sprachzentrums nicht alles entfernen konnten, sprechen wir hier
von einer chronischen Erkrankung, die eine weitere Therapie benötigt."
Lernpunkte
Close
Lernpunkte:
1. Welche molekulargenetischen Marker sind nach der WHO-Klassifikation von 2021 obligat, um die Diagnose
eines Oligodendroglioms stellen zu können?
2. Ist ein Oligodendrogliom prinzipiell IDH-mutiert oder IDH-Wildtyp?
Beim abschließenden Gespräch vor der Entlassung ist Herr Weber bedrückt. "Ich will doch bald wieder vor
meiner Klasse stehen! Mir graut es vor der monatelangen Bestrahlung und Chemotherapie. Fallen mir dann die
Haare aus?"
Sein Arzt lächelt. "Genau das wollen wir Ihnen vorerst ersparen. In unserem Tumorboard haben wir uns
aufgrund Ihres Resttumors zwar gegen ein reines Abwarten entschieden, aber Sie profitieren von einer
medizinischen Revolution."
Der Arzt erklärt ihm, dass er stattdessen eine moderne, zielgerichtete Therapie in Tablettenform bekommt –
den IDH-Inhibitor Vorasidenib. Dieses Medikament bremst das Tumorwachstum gezielt aus und kann die harte
Radiochemotherapie um Jahre hinauszögern.
Sichtlich erleichtert und voller Zuversicht packt Herr Weber seine Tasche. Wenig später unterrichtet er
wieder seine Gymnasialschüler, als wäre nie etwas gewesen.
Lernpunkte
Close
Lernpunkte:
1. Was ist der genaue Wirkmechanismus von Vorasidenib und für welche Patienten ist es zugelassen?
2. Wann wäre nach Leitlinie bei einem Low-Grade Gliom ein reines "Wait and Scan" gerechtfertigt?
3. Was sind die potenziellen Spätfolgen einer frühen Radiochemotherapie, die man durch IDH-Inhibitoren
hinauszuzögern versucht?
Hier finden Sie die Antworten und Leitlinienverweise zu allen in den Fällen gestellten
Lernpunkten. Diese Sektion dient primär der Dozentenvorbereitung und der studentischen Selbstkontrolle.
Fall 1 - Neuroonkologie (Glioblastom / Abszess)
Seite 1:
1. Abklärung Erstanfall: Umgehende Bildgebung (präferabel MRT Kopf, alternativ Nativ-CT
zum Akutausschluss Blutung/Infarkt), Labor, EKG, im Verlauf EEG. (Quelle: DGN Leitlinie Erster
epileptischer Anfall).
2. Vorherige Anfälle: Fokale Anfälle (einfach fokal motorisch), da der Patient bei
Bewusstsein blieb.
3. Aktueller Anfall: Fokal beginnend, sekundär generalisierend (bilateral
tonisch-klonisch).
4. Hemiparese nach Anfall: Ja, als sogenannte "Todd'sche Parese" (postiktale
Erschöpfung des motorischen Kortex), bildet sich meist nach 24-48h zurück.
5. Transportindikation: Erster Krampfanfall ist ein Notfall, es muss eine akute
zerebrale Ischämie oder Blutung ausgeschlossen werden.
Seite 2:
1. Akutbehandlung Anfall: Benzodiazepine i.v. (z.B. Lorazepam/Tavor 1-2 mg, alternativ
Diazepam, Midazolam).
2. CT Interpretation: Hypodense, raumfordernde Läsion mit Ödem rechts frontal. DD:
Tumor (Glioblastom, Metastase) oder Hirnabszess.
3. Blutung im CT: Zeigt sich primär hyperdens (hell/weiß) im Gegensatz zum hypodensen
(dunklen) Tumor/Ödem.
4. OP anhand CT: Nein, zur exakten Operationsplanung und Differentialdiagnostik ist
zwingend ein MRT mit Kontrastmittel erforderlich.
Seite 3:
1. Vigilanzminderung: Postiktale Phase, Nebenwirkung der Benzodiazepine (Tavor),
Hirndruck durch zunehmendes Ödem oder beginnende Einklemmung.
2. Abszess-Ausschluss durch Labor: Nein, CRP und Leukozyten können bei einem gut
abgekapselten Hirnabszess vollkommen normal sein.
3. Intubation GCS: Bei GCS < 8 (Schutzreflexe erloschen, Aspirationsgefahr).
4. Indikation NCH: Raumforderung mit drohendem Hirnödem und neurologischem Defizit
bedarf der neurochirurgischen OP-Planung.
Seite 4:
1. Epilepsie Definition (ILAE 2014): Ein einzelner unprovozierter Anfall reicht
aus, wenn das Risiko für weitere Anfälle >60% beträgt. Dies ist bei einer strukturellen
Läsion im MRT (Tumor) der Fall. Die Diagnose Epilepsie ist damit bestätigt.
2. Fachbegriff symptomatische Epilepsie: Epilepsie struktureller Ätiologie.
3. Zunehmende Parese: Progression des vasogenen Hirnödems, postiktale Phase oder
lokales Tumorwachstum.
4. ITS Überwachung: Nicht zwingend bei einem wachen, kreislaufstabilen Patienten
ohne akute Hirndruckzeichen.
5. Untersuchung: cMRT mit Kontrastmittel und Diffusionswichtung (DWI) zum
Ausschluss eines Abszesses.
Seite 6 (Tumor-Zweig):
1. Dexamethason: Zur Reduktion des tumorbedingten vasogenen Perifokalödems
(Besserung der Schrankenfunktion).
2. Ödem-Typen: Vasogen (Blut-Hirn-Schranke defekt, bei Tumor/Abszess), Zytotoxisch
(Zellschwellung bei Ischämie), Interstitiell (Hydrozephalus).
3. Zytotoxisches Ödem & Cortison: Nein, Cortison wirkt primär am vasogenen
Ödem.
4. WHO 2021 Klassifikation: Integrierte histologische und molekulargenetische
Einteilung (arabische statt römische Ziffern, Grad 1-4).
5. Hochauflösungssequenz: MPRAGE/T1-3D-Datensatz dient als Grundlage für die
intraoperative Neuronavigation.
Seite 7 (Tumor-Zweig):
1. Intraop Elektrophysiologie: Motorisch evozierte Potenziale (MEP) und SSEP,
subkortikale Stimulation. Dient der Identifikation und Schonung der Pyramidenbahn.
2. Marker: MGMT-Promotor-Methylierung prognostiziert ein besseres Ansprechen auf
Temozolomid (Alkylantien). IDH-Mutation ist ein starker positiver prognostischer Marker.
3. Stupp-Schema: Fraktionierte Radiotherapie (60 Gy) plus zeitgleiche Chemotherapie
(Temozolomid), gefolgt von Erhaltungschemotherapie.
4. TTFields: Tumor Treating Fields (Optune), eine physikalische Therapieform mit
elektrischen Wechselfeldern, die ergänzend eingesetzt wird.
Seite 6a/7a (Abszess-Zweig):
1. Antibiose präoperativ: Wird vorerst weggelassen, um den Erregernachweis aus dem
intraoperativ gewonnenen Eiter nicht zu verfälschen.
2. Häufigste Erreger: Streptokokken und Staphylokokken.
3. Fokussuche: Zahnstatus (OPG), Nasennebenhöhlen, Herz (Echokardiographie/TEE zum
Ausschluss Endokarditis).
4. Antibiose Dauer: Meist 6 bis 8 Wochen.
5. Risikofaktoren: Immunsuppression, Endokarditis, chronische Sinusitis, angeborene
Herzfehler (Rechts-Links-Shunt).
Fall 2 - Vaskuläre Neurochirurgie (SAB)
Seite 1:
1. Leitsymptome SAB: Plötzlicher Vernichtungskopfschmerz (Donnerschlagkopfschmerz),
Nackensteifigkeit (Meningismus), Übelkeit/Erbrechen, evtl. Bewusstseinsverlust.
2. Skalen: Hunt & Hess (klinisches Bild), WFNS (GCS und Parese).
3. Diagnostik: Nativ-CT Kopf als erste Akutdiagnostik.
Seite 2:
1. Fisher-Graduierung: CT-Klassifikation (Grad 1-4) zur Einschätzung des Risikos für
sekundäre Vasospasmen anhand der Blutmenge.
2. Kalziumantagonist: Nimodipin. Ziel ist die Neuroprotektion und Prophylaxe sekundärer
Ischämien (Vasospasmus).
3. Blutdruck <160 mmHg: Das Aneurysma ist noch offen. Höhere Drücke erhöhen das Risiko
einer tödlichen Reblutung drastisch.
4. Nimodipin oral: Laut Leitlinie wird die orale Gabe bevorzugt, da die
i.v.-Gabe häufiger zu systemischem Blutdruckabfall führt, was die zerebrale Perfusion
gefährdet.
5. CT-negativ: Bei weiterhin hohem klinischen Verdacht auf SAB und unauffälligem CT muss zwingend eine Lumbalpunktion erfolgen (Nachweis von Xanthochromie/Siderophagen).
Seite 3:
1. Clipping vs. Coiling: Coiling ist oft 1. Wahl. Clipping wird bevorzugt bei
sehr breitem Aneurysmahals, Einbezug von Gefäßästen oder großen raumfordernden
intracerebralen Hämatomen.
2. Rolle der DSA: Goldstandard. Sie zeigt die Gefäßanatomie, den Aneurysmahals
und Gefäßabgänge millimetergenau zur Planung des operativen oder endovaskulären
Vorgehens.
Seite 4:
1. Vasospasmus-Zeitfenster: Tag 4 bis 14 nach dem Blutungsereignis (Maximum um
Tag 7-10).
2. TCD (Doppler): Nicht-invasives Bettseiten-Monitoring zur Messung der
Blutflussgeschwindigkeit. Hohe Geschwindigkeiten indizieren Gefäßengstellungen
(Spasmus).
3. Differentialdiagnosen Verschlechterung: Sekundäre Ischämie (DCI durch
Vasospasmus), Hydrozephalus (Liquoraufstau durch Blut), Reblutung, Hyponatriämie,
epileptischer Anfall.
Seite 5:
1. Therapie symptomatischer Vasospasmus: Induzierte Hypertension (z.B. Gabe von
Noradrenalin) zur Steigerung des Perfusionsdrucks bei strenger Normovolämie.
2. Endovaskuläre Intervention: Wenn die induzierte Hypertension nicht ausreicht
und Ischämien drohen (Spasmolyse mittels intraarteriellem Nimodipin oder
Ballonangioplastie).
3. Prognose: Die Letalität ist hoch. Bei Überlebenden verbleiben häufig
neurokognitive oder psychische Defizite, selbst wenn sich motorische Paresen gut
zurückbilden.
Fall 3 - Neuroonkologie (Glioblastom)
Seite 1:
1. DD Hemiparese: Ischämischer Schlaganfall, intrazerebrale Blutung (ICB), Hirntumor,
Hirnabszess, MS-Schub.
2. Nächster Schritt: CCT (Nativ-CT Kopf) zur Akutdiagnostik.
Seite 2:
1. CCT Befund: Hypodense Raumforderung rechts frontal mit perifokalem Ödem.
2. Blutung vs. Tumor: Eine frische Blutung ist hyperdens (weiß). Tumore und Ödeme sind
meist hypodens (dunkelgrau).
Seite 3:
1. Nächster Schritt: MRT Kopf mit Kontrastmittel.
2. DD: Malignes Gliom (Glioblastom), Hirnmetastase.
Seite 4:
1. OP Risiken: Blutung, Infektion, epileptische Anfälle, Verschlechterung der
Hemiparese.
2. Lagebeschreibung: Rechts frontal/präzentral.
3. Funktionelle Areale: Motorkortex (Gyrus praecentralis, Pyramidenbahn).
4. Alternativen: Stereotaktische Biopsie (falls offene Resektion nicht möglich).
5. Präop Vorbereitung: Aufklärung, Nüchternheit, Dexamethason, evtl.
Antiepileptika.
6. Dexamethason Indikation: Vasogenes Ödem bei Tumoren und Abszessen (nicht bei Trauma
oder Ischämie!).
7. Andere Medikamente Ödem: Osmotische Diuretika (Mannitol) in der akuten
Einklemmungssituation.
Seite 5:
1. Fluoreszenz (5-ALA): Tumor nimmt den Stoff auf und wandelt ihn in Porphyrine um.
Unter blauem Licht leuchtet der Tumor pink/rot, gesundes Gewebe blau. Hilft bei der
Randzonenresektion.
2. Elektrophysiologie: Dauerhafte Kontrolle der Integrität der Pyramidenbahn mittels
MEP/SSEP.
3. Geräte: Neuronavigation, intraoperativer Ultraschall (iUS), CUSA.
Seite 6:
1. Resektionsausmaß: Eine möglichst vollständige Resektion ("maximal safe resection")
korreliert signifikant mit einem längeren Gesamtüberleben.
2. Postop MRT (< 72h): Danach entsteht chirurgisch bedingtes Granulationsgewebe, das
Kontrastmittel aufnimmt und fälschlicherweise als Resttumor interpretiert werden
könnte.
3. WHO 2021 Glioblastom: Muss zwingend IDH-Wildtyp sein. (Ein IDH-mutierter
Grad 4 Tumor ist nach aktueller Nomenklatur ein Astrozytom).
4. MGMT: Die MGMT-Promotor-Methylierung ist der wichtigste prädiktive Marker
für das Ansprechen auf die Chemotherapie mit Temozolomid.
Fall 4 - Schmerzen der Hand (KTS / HWS)
Seite 1:
1. DD Kribbelparästhesien Hand: Karpaltunnelsyndrom (KTS), Zervikale Radikulopathie
(z.B. C6), Polyneuropathie, Sulcus-ulnaris-Syndrom, Pronator-teres-Syndrom.
2. Radikulopathie vs Neuropathie: KTS betrifft nur Daumen, Zeige- und Mittelfinger
volar (N. medianus). Eine C6-Radikulopathie umfasst den ganzen Dermatom-Streifen über den
radialen Unterarm/Bizeps, hat oft begleitende Nackenschmerzen und eine Abschwächung des
Bizepssehnenreflexes.
Seite 2:
1. Verdachtsdiagnosen: A = Karpaltunnelsyndrom (positives Hoffmann-Tinel und Phalen). B
= Zervikale Radikulopathie C6 rechts mit zusätzlicher zervikaler Myelopathie (gesteigerte
Reflexe der Beine, Klonus).
2. Nächste Schritte: A -> Überweisung zum Neurologen für NLG/EMG. B -> Überweisung ins
MRT HWS.
Fall A (KTS) - Seite 3:
1. Konservative Dauer: Versuch mit nächtlicher Schienung über ca. 3 Monate laut
AWMF-Leitlinie.
2. Beendigung: Bei pathologischem NLG-Befund, dauerhafter Gefühlsstörung,
Thenarmuskelatrophie oder therapieresistenten starken Schmerzen ist die Indikation zur OP
gegeben (hier erfüllt).
Fall A - Seite 4:
1. Präop Untersuchungen: Elektrophysiologie (Nervenleitgeschwindigkeit / NLG).
2. Therapien: Konservativ (Volare Schiene, lokale Cortisoninjektion). Operativ (Offene
Spaltung, Endoskopische Spaltung).
Fall A - Seite 5:
1. Gespaltene Struktur: Ligamentum carpi transversum (Retinaculum flexorum).
2. Offen vs Endo: Offen hat ein geringeres Risiko für Nervenverletzungen und ist der
Goldstandard. Endoskopisch hinterlässt eine kleinere Narbe und erlaubt teils schnellere
Arbeitsfähigkeit, hat aber eine höhere Komplikationsrate.
3. Ambulant: Es ist ein sehr kurzer, oberflächlicher Eingriff, der gut in
Lokalanästhesie oder Plexusanästhesie durchgeführt werden kann.
Fall A - Seite 6:
1. Nachbehandlung: Keine Immobilisation! Freie Beweglichkeit der Finger sofort fördern
(ggf. Ergotherapie), Vollbelastung erst nach ca. 3 Wochen.
2. Symptomrückbildung: Schmerzen (vor allem nachts) bessern sich sofort.
Taubheit/Hypästhesie und Paresen benötigen Monate zur Regeneration und können teils irreversibel
sein.
3. Pseudoneurom: Durch den chronischen mechanischen Druck entsteht proximal der
Engstelle eine reaktive sanduhrförmige Verdickung des Nervs.
Fall B (HWS) - Seite 3a:
1. T2-Myelopathiesignal: Eine Hyperintensität im Rückenmark, die auf ein
intra-medulläres Ödem oder Gliose durch chronische Kompression hinweist. Dies ist eine absolute
OP-Indikation!
2. Motorischer Ausfall C6: Schwäche bei Beugung im Ellenbogengelenk (M. biceps brachii
/ M. brachioradialis).
Fall B - Seite 4a:
1. Zugang HWS: Standardmäßig ventral (von vorne) als ACDF (Anterior Cervical Discectomy
and Fusion).
2. Alternative: Konservative Therapie ist bei bestehender Myelopathie
(Rückenmarkschaden) nicht zu empfehlen. Alternativer OP-Zugang: Dorsale Laminektomie (hier
ungünstig wegen ventralem Bandscheibenvorfall).
Fall B - Seite 5a:
1. Ventraler Zugang: Schnitt längs oder quer am vorderen Hals. Präparation in der
Schicht zwischen dem Gefäß-Nerven-Strang (A. carotis, V. jugularis) lateral und
Trachea/Ösophagus medial bis zur Halswirbelsäule. Unter Mikroskop wird die Bandscheibe komplett
entfernt (Diskoidektomie), das Rückenmark entlastet und abschließend ein Platzhalter (Cage) als
Fusion eingesetzt.
Fall 5 - Bandscheibenvorfall (LWS)
Seite 1:
1. Nervenwurzel: L5 (Dermatom umfasst die Oberschenkelaußenseite, vordere/äußere Wade
bis zur Großzehe).
2. Konservative Dauer: Laut Leitlinien bei radikulärem Schmerz (ohne motorische/kaudale
Ausfälle) initial 6-8 Wochen.
Seite 2:
1. Absolute OP-Indikationen (Red Flags): Kauda-Syndrom (Reithosenanästhesie,
Blasen-Mastdarm-Störungen) sowie frische hochgradige (Kraftgrad < 3/5) oder progrediente
Paresen.
2. Muskel bei L5: M. tibialis anterior (Fußheber) und M. extensor hallucis longus
(Großzehenheber).
Seite 4:
1. Notfall Parese: Je länger die Kompression auf den Nerv andauert (Ischämie der
Wurzel), desto höher ist das Risiko eines irreversiblen Schadens (bleibende
Fußheberschwäche/Steppergang).
2. OP-Zugang: Dorsaler Zugang, interlaminäres Fenster (ggf. Flavektomie/kleine
Laminektomie), Darstellen der Nervenwurzel und mikrochirurgische Sequestrektomie.
Seite 5:
1. Prognose Erholung: Bei frühzeitiger (< 48h) operativer Dekompression ist die
Prognose der motorischen Erholung sehr gut.
2. Nachsorge: Frühmobilisation, Rumpfstabilisierung (Physiotherapie),
Rückenschule zum Erlernen wirbelsäulengerechten Verhaltens im Alltag, Vermeiden von
schwerem Heben in Rumpfbeugung in den ersten 6 Wochen.
Fall 6 - Neuroonkologie (Low-Grade Gliom)
Seite 1:
1. DD Erstanfall junger Erwachsener: Hirntumor (speziell niedriggradige Gliome
manifestieren sich fast immer primär durch Krampfanfälle!), SAB, Enzephalitis, Ischämie,
Hypoglykämie, Intoxikation.
2. MRT Notwendigkeit: Ein unauffälliges CT schließt eine strukturelle Ursache nicht aus
(speziell LGGs sind im CT oft isodens/unsichtbar). MRT mit KM ist der Goldstandard bei
Erstdiagnose einer Epilepsie im Erwachsenenalter.
Seite 2:
1. MRT-Zeichen LGG: T2/FLAIR hyperintens, typischerweise keine
Kontrastmittelaufnahme (im Gegensatz zum Glioblastom), kaum perifokales Ödem, wenig
Masseneffekt.
2. Funktionelle Areale links frontal: Primär motorischer Kortex (Gyrus praecentralis,
v.a. Gesicht/Arm), motorisches Sprachzentrum (Broca-Areal, Gyrus frontalis inferior),
prämotorischer Kortex, SMA (Supplementary Motor Area).
Seite 3:
1. Indikation Wach-OP: Eine Läsion befindet sich unmittelbar in oder angrenzend an
"eloquente" Areale (wie hier dem Sprachzentrum), deren Verletzung zu schweren neurologischen
Defiziten führen würde.
2. Rolle der Logopäden: Führen intraoperativ (beim wachen Patienten) standardisierte
Sprachtests (Zählen, Bilder benennen, Lesen) durch. Der Chirurg stimuliert gleichzeitig den
Kortex elektrisch – stoppt der Patient beim Sprechen, ist das Areal identifiziert und muss
geschont werden.
3. Maximal sichere Resektion: Ein radikales onkologisches Vorgehen (Entfernung)
verlängert signifikant das Überleben, darf aber nie zu Lasten der Lebensqualität (z.B. Erzeugung
einer Aphasie oder Parese) gehen, da ein schweres Defizit das Gesamtüberleben indirekt wieder
stark verkürzt.
Seite 4:
1. Molekulare Marker Oligodendrogliom (WHO 2021): Zwingend erforderlich sind sowohl der
Nachweis einer IDH-Mutation als auch einer 1p/19q-Kodeletion.
2. IDH-Status: Ein Oligodendrogliom ist per Definition immer
IDH-mutiert. Ein IDH-Wildtyp Oligodendrogliom gibt es in der neuen Klassifikation nicht mehr.
Seite 5:
1. Wirkmechanismus Vorasidenib: Ein oraler, liquorgängiger Inhibitor der mutierten
IDH1/2-Enzyme. Er blockiert die Produktion des Onkometaboliten (2-HG) und verzögert das
Tumorwachstum signifikant. Zugelassen bei IDH-mutierten Gliomen Grad 2 mit Resttumor nach
OP.
2. "Wait and Scan": Eine reine Verlaufsbeobachtung ist nur bei sogenannten
"Low-Risk"-Patienten vertretbar (meist < 40 Jahre alt und komplette
Tumorresektion ohne Restnachweis).
3. Spätfolgen Radiochemo: Chronische Strahlennekrosen, kognitive Einbußen
(Leukoenzephalopathie), endokrinologische Ausfälle und das Risiko sekundärer Neoplasien
(z.B. strahleninduzierte Meningeome oder Leukämie durch Chemotherapie nach Jahren).